
SEPLIFE ®Alles, was Sie über Ionenaustauschchromatographie wissen müssen
Einführung in die Ionenaustauschchromatographie:
Die Ionenaustauschchromatographie ist eine Säulenchromatographie-Methode, die die Unterschiede in den elektrostatischen Kräften zwischen den austauschbaren Ionen am Ionenaustauscher und den verschiedenen Ionen im umgebenden Medium nutzt und die Trennung durch ein Austauschgleichgewicht erreicht. Sie zeichnet sich durch hohe Empfindlichkeit, Reproduzierbarkeit, gute Selektivität und schnelle Analysengeschwindigkeit aus und gehört heute zu den am häufigsten angewandten Chromatographie-Methoden.
1848 entdeckten Thompson et al. das Phänomen des Ionenaustauschs bei der Untersuchung des Austauschs alkalischer Substanzen im Boden. In den 1940er Jahren kamen Polystyrol-Ionenaustauscherharze mit stabilen Austauscheigenschaften auf den Markt. In den 1950er Jahren hielt die Ionenaustauschchromatographie Einzug in die Biochemie und wurde zur Analyse von Aminosäuren eingesetzt. Auch heute noch ist die Ionenaustauschchromatographie eine gängige chromatographische Methode in der Biochemie und wird häufig zur Trennung und Reinigung verschiedener biochemischer Substanzen wie Aminosäuren, Proteine, Zucker, Viren und Nukleotide verwendet.
Der Ionenaustauschprozess:
Die Reaktion zwischen dem Ionenaustauscher und den Ionen oder ionischen Verbindungen in der Lösung erfolgt hauptsächlich durch Ionenaustausch. Die durchgeführte Ionenaustauschreaktion ist reversibel. Unter der Annahme, dass RA den Kationenaustauscher darstellt, kann das in der Lösung dissoziierte Kation A+ eine reversible Austauschreaktion mit dem Kation B+ in der Lösung eingehen, und die Reaktionsgleichung lautet:
RA + B+ →RB + A+
Die Reaktion erreicht das Gleichgewicht extrem schnell, und die Gleichgewichtsverschiebung folgt dem Massenwirkungsgesetz.
Die Selektivität eines Ionenaustauschers kann durch die Gleichgewichtskonstante seiner Reaktion ausgedrückt werden:
K=[RB][A+]/[RA][B+]
✔Wenn [A+] gleich [B+] in der Reaktionslösung ist, dann ist K=[RB]/[RA].
✔Wenn K > 1, also [RB] > [RA], bedeutet dies, dass die Bindungskraft des Ionenaustauschers zu B+ größer ist als die zu A+.
✔Wenn K=1 ist, bedeutet auch [RB]=[RA], dass der Ionenaustauscher die gleiche Bindungskraft zu A+ und B+ hat;
✔Wenn K
✔Der K-Wert ist ein Parameter, der die Bindungskraft oder Selektivität des Ionenaustauschers gegenüber verschiedenen Ionen widerspiegelt. Daher wird der K-Wert als Selektivitätskoeffizient des Ionenaustauschers für A+ und B+ bezeichnet.
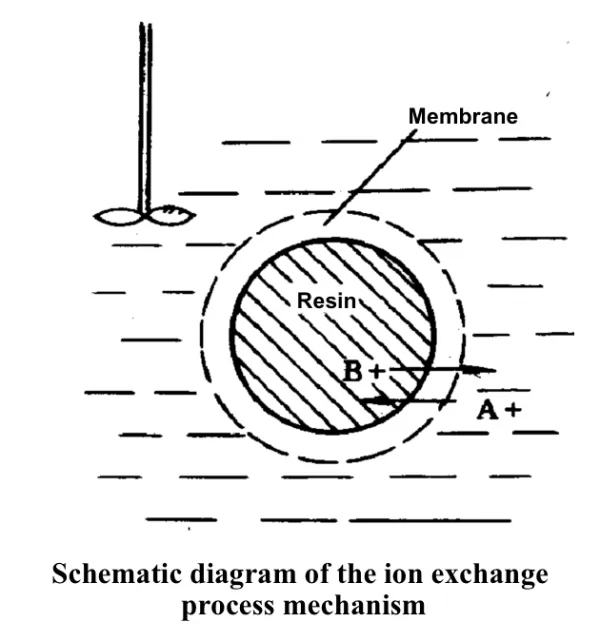
Mechanismus des Ionenaustauschs:
A+ diffundiert aus der Lösung zur Harzoberfläche.
A+ dringt von der Oberfläche des Harzes in das aktive Zentrum im Inneren des Harzes ein.
A+ unterliegt einer Metathesereaktion mit RB am aktiven Zentrum.
Das desorbierte Ion B+ diffundiert vom Inneren des Harzes zur Oberfläche des Harzes.
B+-Ionen diffundieren von der Harzoberfläche in die Lösung.
Der geschwindigkeitsbestimmende Faktor für die Austauschrate ist die Diffusionsrate, die in verschiedenen Trennsystemen durch interne oder externe Diffusion gesteuert werden kann.
Faktoren, die den Ionenaustauschprozess beeinflussen:
✔Partikelgröße: Je kleiner, desto schneller
✔Vernetzungsgrad: geringer Vernetzungsgrad, hohe Austauschgeschwindigkeit
✔Temperatur: Je höher die Temperatur, desto schneller; Dies hängt mit der Zunahme des Diffusionskoeffizienten zusammen.
✔Ionenvalenz: Je höher die Valenz, desto langsamer die Diffusionsrate.
✔Ionengröße: Je kleiner, desto schneller
✔ Rührgeschwindigkeit: Bis zu einem gewissen Grad gilt: Je größer, desto schneller
✔Lösungskonzentration: Wenn die Austauschrate durch Diffusion bestimmt wird, ist die Austauschrate umso höher, je größer die Konzentration ist.
Prinzip des Ionenaustauschs:
Bei Verwendung eines Kationenaustauscherharzes wird die positiv geladene Substanz gegen H⁺ ausgetauscht und an das Harz gebunden. Bei Verwendung eines Anionenaustauscherharzes kann die negativ geladene Substanz gegen OH⁻ ausgetauscht und an das Harz gebunden werden.
Es gibt Unterschiede im Grad der Festigkeit der Stoffkombinationen auf dem Harz, und die Komponenten des Gemisches können durch Auswahl eines geeigneten Elutionsmittels nacheinander eluiert werden, um die Trennung und Reinigung zu erreichen.
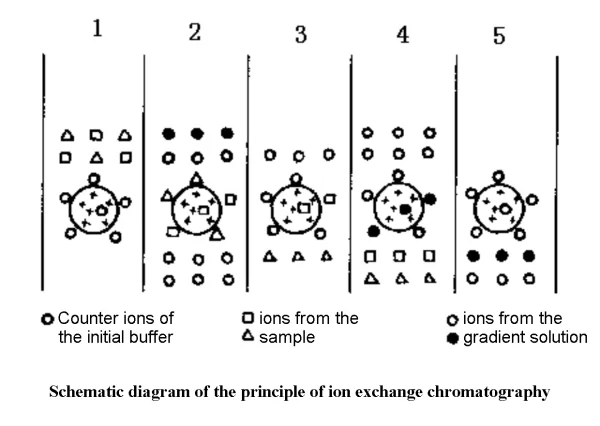
✔1. Äquilibrierungsphase: Kombination von Ionenaustauscher und Gegenionen
✔2. Adsorptionsphase: Austausch von Sonde und Gegenionen
✔3. Desorptionsphase: Die Gradientenpufferlösung wäscht zuerst die schwach adsorbierten Substanzen ab und anschließend die stark adsorbierten Substanzen.
✔4. Regenerationsphase: Vollständiges Spülen mit der ursprünglichen Ausgleichslösung, die wiederverwendet werden kann.
Ionenaustauscher-Chromatographieharze:
Die geladenen Gruppen der Kationenaustauscher sind negativ geladen, die Gegenionen dagegen positiv. Sie können Austauschreaktionen mit Kationen oder positiv geladenen Verbindungen in Lösung durchführen.
Nach der Stärke der geladenen Gruppe kann man in drei Typen einteilen: starke Säuren (Gruppe mit Sulfonsäure, R-SO3H), mittelstarke Säuren (mit Phosphorsäuregruppe oder Phosphoriger Säuregruppe, R-PO3H2) und schwache Säuren (mit Carboxylgruppe und Phenolharz, R-COOH oder R-Benzolring-OH).
Beim Austausch dieser Ionenaustauscher werden die Wasserstoffionen durch Fremdkationen ersetzt, wie in der folgenden Formel dargestellt:
R-COOH+Na+=R-COONa++H+
Der Anionenaustauscher wird durch Einführung von quaternären Aminen [-N (CH3) 3], tertiären Aminen [-N (CH3) 2], sekundären Aminen [-NHCH3] und primären Aminen [-NH2] Gruppen auf der Matrix gebildet.
Nach dem unterschiedlichen Alkalitätsgrad der Aminogruppen kann man sie in drei Typen unterteilen: stark basisch (einschließlich quaternärer Aminogruppen), schwach basisch (einschließlich tertiärer und sekundärer Aminogruppen) und mittelstark basisch (mit sowohl stark basischen als auch schwach basischen Gruppen).
Beim Austausch mit Ionen in Lösung ergibt sich folgende Reaktionsformel:
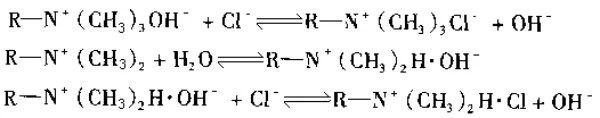
Weitere Informationen zu den spezifischen Arten von Ionenaustauscher-Chromatographieharzen finden Sie in unserem nächsten Artikel über Ionenaustauschchromatographie.















